核酸合成の手順と使用試薬 -ホスホロアミダイト法-
目次
核酸合成について
核酸合成とは核酸(DNA・RNA)を人工的に合成する方法です。中でも核酸医薬品で利用されるオリゴヌクレオチドの合成には、液相法と固相法が用いられています。
従来、オリゴヌクレオチドの合成には液相法が用いられてきました。しかし、この方法では各工程で抽出・精製が必要で、合成に長い時間と高い熟練度が求められるデメリットがあります。
一方、ホスホロアミダイト法を中心とする固相法では1サイクルでの合成手法が確立されており、自動合成装置を用いるため比較的容易に合成を行うことができます。
ホスホロアミダイト法とは
ホスホロアミダイト法とは、1980年代に開発された核酸合成方法です。
核酸を化学合成する際には核酸ユニットを任意の配列に従って一つ一つ繋げる必要があります。
ホスホロアミダイト法は、その過程が比較的容易であり効率的に進められるため、オリゴヌクレオチド合成の中でも主流となっています。
次世代の分子標的薬として注目されている核酸医薬品の開発には、核酸の合成が重要な役割を果たしており、これが生物学的な応用の基盤となっています。
核酸・核酸医薬品については下記ページでも詳しく解説しています。
ホスホロアミダイト法の手順と必要な試薬
ホスホロアミダイト法では、CPG(Controlled Pore Glass)にエステル結合で連結された核酸を最初の核酸(3’末端の核酸)として固相合成がスタートします。

ホスホロアミダイト法では、合成サイクルが[合成する核酸の塩基数-1]回繰り返されるため、1サイクルごとの反応収率は非常に高い水準(99~99.5%以上)が求められます。1サイクルごとの反応効率を100%に近づけるためには、最適化された反応条件のもと、純度の高い合成用試薬や溶媒類を使用する必要があります。
縮合反応や固相の洗浄操作:アセトニトリル
ホスホロアミダイト法では溶媒に含まれる水分により収率が低下することから、極めて高い脱水条件下で反応を進行させる必要があるため、縮合反応や固相の洗浄操作にアセトニトリルが使用されます。
水分量が10ppm以下のアセトニトリルであれば、縮合反応に問題なく使用できるとされています。
ホスホロアミダイトユニット
DNA鎖の伸長反応(縮合反応)には、3価の亜リン酸部位を構造中に持つホスホロアミダイトユニットを用い、縮合反応を行います。
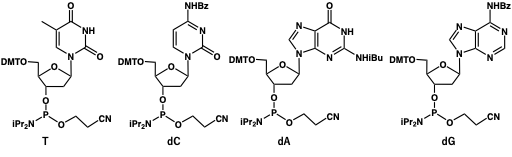
5’水酸基の保護には、弱酸で脱保護可能なジメトキシトリチル基が利用されています。また、核酸塩基のアミノ基は塩基性条件下で脱保護可能なアシル基で保護されています。
アデニンとシトシンのアミノ基にはベンゾイル基、グアニンのアミノ基にはイソブチリル基を保護基として使用するのが一般的です。マイルドな塩基性条件で脱保護を行いたい場合には、アデニンとグアニンのアミノ基にはpac基、シトシンのアミノ基にはアセチル基を保護基として使用することもあります。
ホスホロアミダイトユニット中のP-N結合は、テトラゾールで活性化されることにより固相上の水酸基と反応します。そのため、亜リン酸部位に由来するホスホロアミダイトユニットの不斉については、S型とR型の混合物として利用することが可能です。
DMT基の脱保護:デブロック剤
ホスホロアミダイトユニット(=ヌクレオシド)は5’位がDMT基(ジメトキシトリチル基)で保護されています。次工程のカップリングでは5’位を反応点とするため、事前に脱保護が必要です。
DMT基の脱保護には「トリクロロ酢酸 ジクロロメタン溶液」「ジクロロ酢酸 トルエン溶液」が利用されます。濃度が高いほどより効率的にDMT基の脱保護が進められます。
DMT基が脱保護された際に生じる橙色を追跡することで、反応の完結を目視により確認することが可能なステップです。効率よく反応を進行させるためには、脱水された溶媒を使用する必要があります。
| 品名 | 品番 | 容量 |
|---|---|---|
|
3w/v%トリクロロ酢酸 ジクロロメタン溶液 BioSyn™, Detritylation Reagent, for DNA/RNA synthesis |
BR6054X2 | 2L×4 |
| BR605-4X2.5L | 2.5L×4 | |
|
10%ジクロロ酢酸 トルエン溶液 BioSyn™, Detritylation Reagent, for DNA/RNA synthesis |
BR676ADAK-4 | 4L×4 |
| BR6764X4 | 4L×4 | |
| BR676-4X2.5L | 2.5L×4 | |
|
3%ジクロロ酢酸 トルエン溶液 BioSyn™, Detritylation Solution, for DNA/RNA synthesis |
SR6744X4 | 4L×4 |
カップリング:アクチベーター(活性化剤)
DMT基が脱保護されたホスホロアミダイトユニットを連結(カップリング・縮合反応)するには、反応を活性化させるアクチベーター(活性化剤)が必要です。アクチベーターにはテトラゾール(ETT)やDCI(ジシアノイミダゾール)などが用いられます。
| 品名 | 品番 | 容量 |
|---|---|---|
|
0.5M ETT アセトニトリル溶液 BioSyn™, Activator Reagent, for DNA/RNA synthesis |
BR7252X1 | 1L×2 |
| BR7254X2.5 | 2.5L×4 | |
|
0.25M ETT アセトニトリル溶液 BioSyn™, Activator Reagent, for DNA/RNA synthesis |
BR7214X2 | 2L×4 |
| BR721-4X4L | 4L×4 | |
| SR7212X1 | 1L×2 | |
| SR721-2.5 | 2.5L×4 |
キャッピング剤
ホスホロアミダイト試薬を利用した縮合反応は非常に高収率で進行しますが、未反応の水酸基(5'ヒドロキシル基)は必ず残ってしまいます。そのため、以降の縮合反応から未反応の水酸基を除外するために、水酸基を不活性な誘導体にアセチル化するキャッピング反応が必要となります。
キャッピング反応には「無水酢酸 ピリジン溶液」、また求核触媒には1-メチルイミダゾールを用います。1-メチルイミダゾールを「無水酢酸 ピリジン溶液」にあらかじめ混合すると副反応が生じるため、1-メチルイミダゾールの溶液はキャップ化反応の直前に、無水酢酸と混合する必要があります。
| 品名 | 品番 | 容量 |
|---|---|---|
|
Capping Reagent Kit BioSyn™, for DNA/RNA Synthesis, contains 40% Acetic Anhydride/ 60% Acetonitrile (BR643) and 60% 2,6-Lutidine / 40% Acetonitrile (BR645) |
BR6482.5 | 2.5L×2 |
|
10v/v%無水酢酸、10v/v%2,6-ルチジン、80v/v%THF BioSyn™, Capping Reagent, for DNA/RNA synthesis |
BR6404X2 | 2L×4 |
| BR640-4X2.5L | 2.5L×4 | |
| BR640-4X4L | 4L×4 | |
|
Capping Reagent Kit BioSyn™, for DNA/RNA Synthesis, contains 5% Phenoxyacetic Anhydride in Acetonitrile (BR753) and 60% 2,6-Lutidine / 40%Acetonitrile (BR645) |
BR758000 | 1L KIT |
|
20v/v%N-メチルイミダゾール、80v/v%アセトニトリル BioSyn™, Capping Reagent, for DNA/RNA synthesis |
BR6542X1 | 1L×2 |
| BR654X2.5 | 2.5L×4 | |
|
15%N-メチルイミダゾール、アセトニトリル溶液 BioSyn™, Capping Reagent, for DNA/RNA synthesis |
BR6604X4 | 4L×4 |
|
10v/v%N-メチルイミダゾール、90v/v%THF BioSyn™, Capping Reagent, for DNA/RNA synthesis |
BR6514X2 | 2L×4 |
| BR6514X4 | 4L×4 | |
| BR651-4X2.5L | 2.5L×4 | |
|
20%無水酢酸、30%ルチジン、50%アセトニトリル溶液 BioSyn™, Capping Reagent, for DNA/RNA synthesis |
SR6442X1 | 1L×2 |
|
10v/v%無水酢酸、10v/v%ピリジン、80v/v%THF BioSyn™, Capping Reagent, for DNA/RNA synthesis |
BR6414X2 | 2L×4 |
|
20v/v%無水酢酸、80v/v%アセトニトリル BioSyn™, Capping Reagent, for DNA/RNA synthesis |
BR6594X4 | 4L×4 |
酸化剤・硫化剤
縮合反応により生じた不安定3価の亜リン酸トリエステルを酸化させ、安定化させるためには酸化剤・硫化剤が必要です。
固相上で形成された3価の亜リン酸トリエステル結合は、「0.02~0.1Mヨウ素 ピリジン-H2O溶液」により酸化され、天然の核酸と同様に5価のリン酸誘導体へと変換されます。酸化反応は非常に速く、ほぼ定量的に進行します。
核酸医薬品には、天然核酸のバックボーンであるホスホジエステル結合をもつ誘導体以外に、ホスホロチオアート結合が導入された誘導体(PS-oligo)が報告されています。PS-oligoは核酸分解酵素への耐性があるだけでなく、RNaseHの基質にもなることから、アンチセンス核酸の母核として研究が進められてきた歴史があります。このPS-oligoを合成する際には、亜リン酸トリエステルを、酸化剤ではなく硫化剤(Beaucage試薬、DDTT等)により硫化します。
| 品名 | 品番 | 容量 |
|---|---|---|
|
0.05Mよう素 10v/v%水、10v/v%ピリジン、80v/v%アセトニトリル溶液 BioSyn™, Oxidation Reagent, for DNA/RNA synthesis |
BR7612X1 | 1L×2 |
|
酸化剤 BioSyn™, Oxidation Reagent, for DNA/RNA synthesis |
BR6674X4 | 4L×4 |
|
0.05Mよう素 10v/v%水、90v/v%ピリジン溶液 BioSyn™, Oxidation Reagent, for DNA/RNA synthesis |
BR664X4L | 4L×4 |
| BR6642.5 | 2.5L×4 | |
|
0.02Mよう素 2v/v%水、20v/v%ピリジン、78v/v%THF溶液 BioSyn™, Oxidation Reagent, for DNA/RNA synthesis |
BR6634X2 | 2L×4 |
| BR663-4X2.5L | 2.5L×4 | |
| BR6634X4 | 4L×4 | |
|
0.02Mよう素 10v/v%水、20v/v%ピリジン、70v/v%THF溶液 BioSyn™, Oxidation Reagent, for DNA/RNA synthesis |
BR6664X2 | 2L×4 |
| BR666-4X2.5L | 2.5L×4 | |
| SR666-4 | 4L×4 |