- トップページ
- 製品の選び方
- 混合標準溶液(Mix)シリーズライブラリ
- GC/MS混合標準液の分析 前編
GC/MS混合標準液の分析 前編アジレント・テクノロジー株式会社 滝埜 昌彦氏
目次
あわせて読む
GC/MS混合標準液の分析 後編
はじめに
GC-MSはその高い分離能と堅牢性から、残留農薬一斉分析において現在でも広く使用されている。GC-MSの残留農薬多成分一斉分析では、市販の混合溶液等を利用することが多い。それらの混合標準溶液の中には、注入口やカラム内で熱分解を起こす農薬や低感度の農薬も含まれており、必ずしもGC-MSでの測定が最善ではないと考えられる農薬も見られる。
そこで本検討では、GC-MS用混合標準液を用いてLC-MSで測定を行い測定に適しているかの評価を行った。今回の検討では、あくまでLC-MSで測定可能かについ混合標準液を用いて評価した結果であり、定量性や実試料での測定については検討していない。
【実験方法】
LC-MSの測定条件
装置はAgilent Jet Stream(AJS) イオン源を装着したAgilent Technologies製Agilent Ultivo Triple Quadrupole LC/MS システムを使用した。分析用カラムは微小粒子径の逆相カラムであるAgilent Technologies製ZORBAX Eclipse Plus C18 RRHD (100 mm, 2.1 mm, 1.8 μm)を使用し,移動相はメタノール及び2 mM酢酸アンモニウム水溶液を使用した。質量分析計は正/負イオン切り替えダイナミックMRM法(dMRM)を用いて測定を行った。分析条件は表1に示した通りである。
検討した標準品は林純薬工業製、PL2005農薬GC/MS Mix Ⅰ, PL2005農薬GC/MS Mix Ⅱ
PL2005農薬GC/MS Mix Ⅲ, PL2005農薬GC/MS Mix Ⅳ, PL2005農薬GC/MS Mix Ⅴ,
PL2005農薬GC/MS Mix Ⅵ及びPL2005農薬GC/MS Mix 7である。
各農薬混合液の評価は以下の手順で実施した。
- 混合標準液をScanモードで測定
- 各農薬のプロトン化分子またはアンモニウム付加分析のETCでピークの確認
- ピークのマススペクトルの確認
- 各農薬のプロダクトイオンスペクトルを測定
- 最適なプロダクトイオンの選択
- MRMモードでコリジョンエネルギーの最適化
- dMRM法で各農薬混合標準液(100-1ppb)を測定
初めに10 ppm標準混合液を用いてスキャンモードで測定した。
その結果、プロトン化分子又はアンモニウム付加分子(分子質量関連イオン)の抽出イオンクロマトグラム(EIC)でピークが検出でき、そのマススペクトル中上記イオンが明確に観察された農薬は、プロダクトイオンスキャン及びMRM法でMRMトランジション条件の最適化を行った。
各農薬のMRM条件は農薬混合液毎に表2-5に示した。各農薬混合標準液を個別にメタノールで希釈し、100,50,10,5及び1 ppb溶液をdMRM法で測定を行った。各農薬類の測定幅は、ピーク幅の2.5倍に設定した。
表1 LC-MS分析条件

表2 PL2005農薬GC/MS MixⅠ,ⅡのdMRM条件
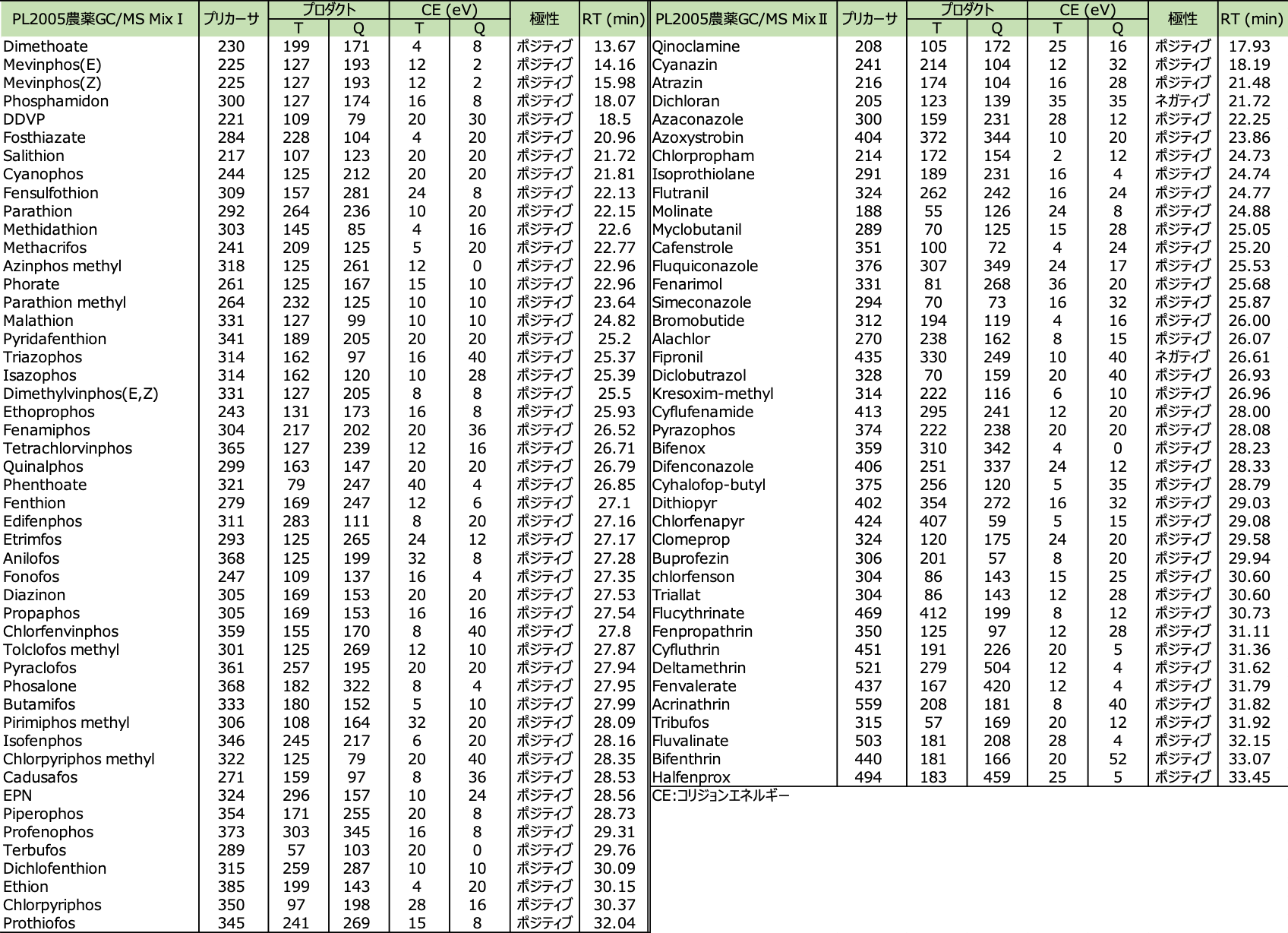
表3 PL2005農薬GC/MS MixⅢ,ⅣのdMRM条件
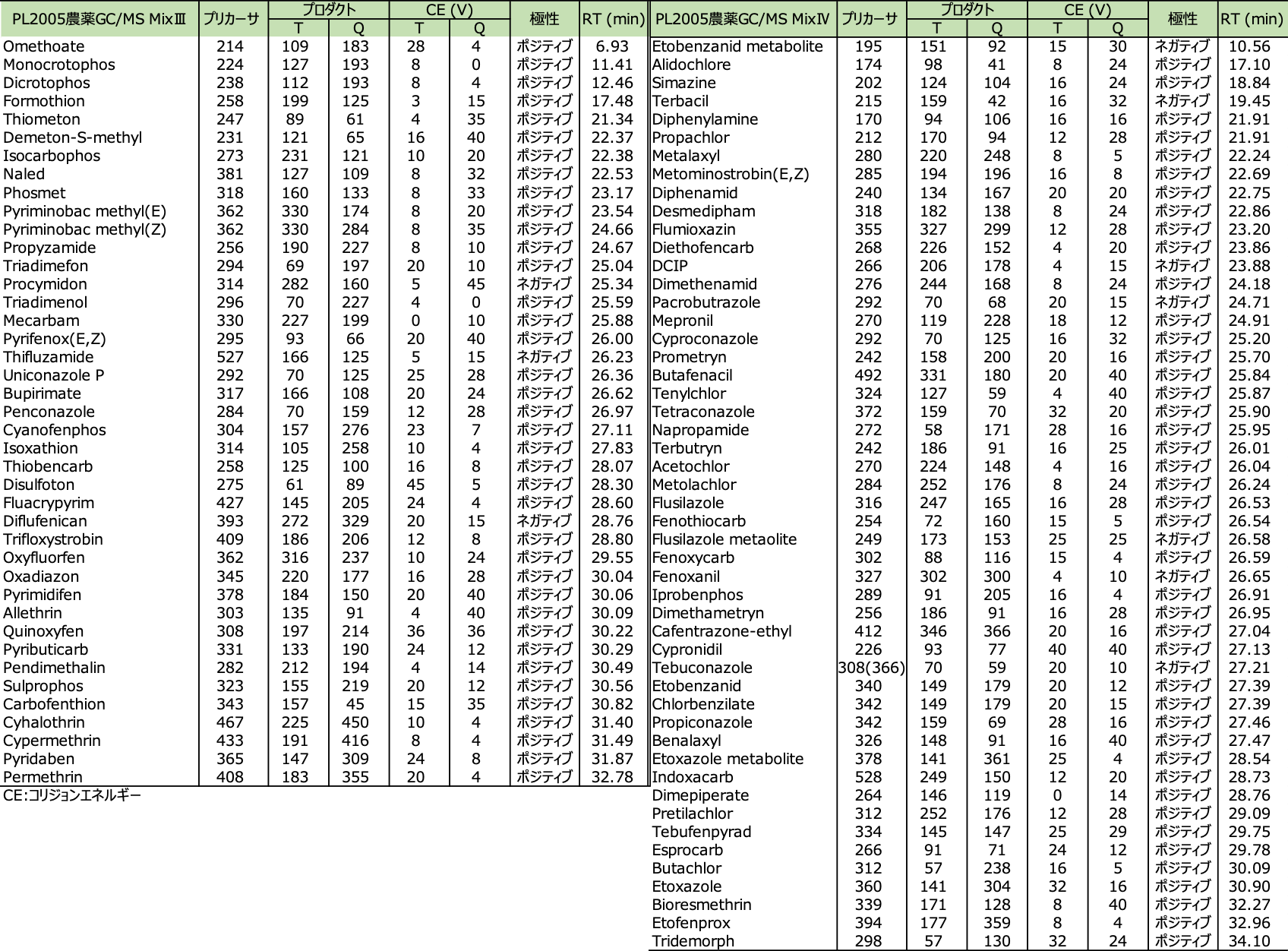
表4 PL2005農薬GC/MS MixⅤ、ⅥのdMRM条件
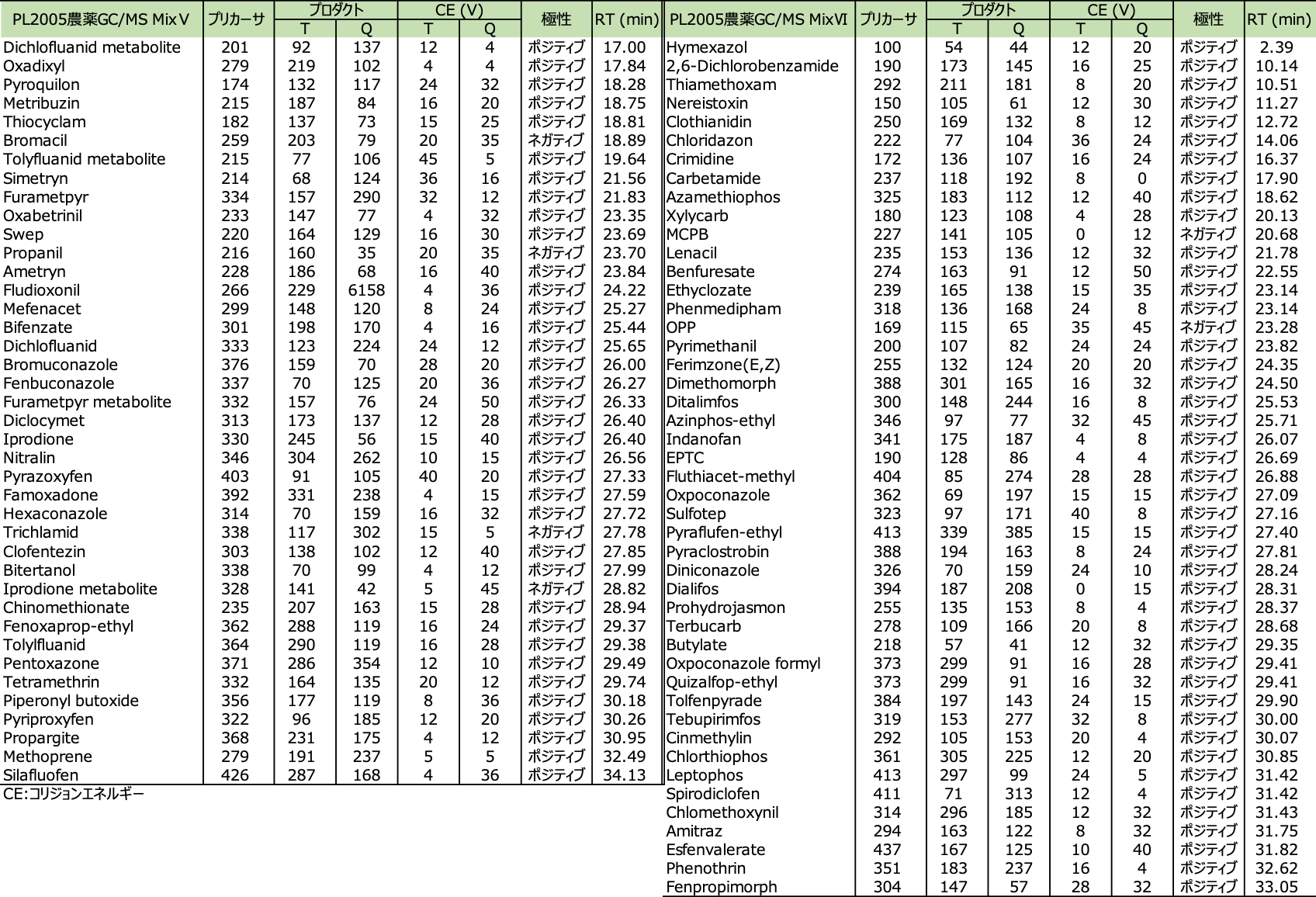
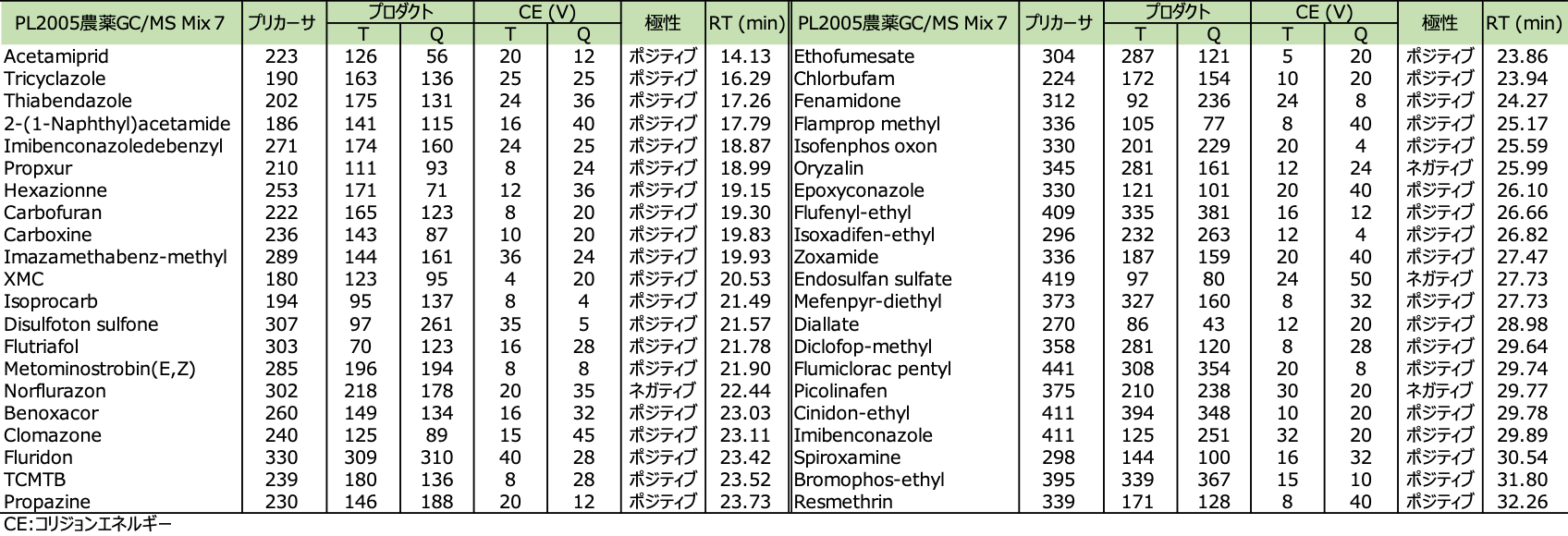
表5 PL2005農薬GC/MS Mix7のdMRM条件
【結果及び考察】
PL2005農薬GC/MS Mixを評価した結果、Scanモードで明確に分子質量関連イオンが確認できなかった農薬は×、MRMクロマトグラムにおいて1 ppbでS/Nが10以下の農薬は△、S/N>10を〇と判定した。結果は以下に示した。
PL2005農薬GC/MS MixⅠ
表6に判定結果、図1に1 ppbでのMRMクロマトグラムを示した。51農薬中フェニトロチオン以外は測定が可能で、パラチオンメチル(10 ppbで測定可能)以外の農薬は1 ppbでS/N>10で検出可能であった。
表6 GC/MS MixⅠの農薬及び判定結果
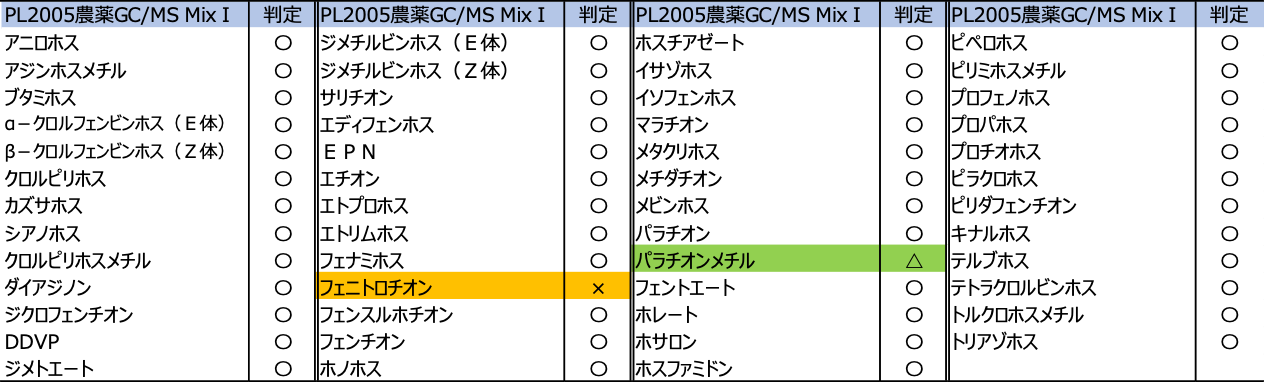

図1-1 GC/MS MixⅠ(1 ppb)のMRMクロマトグラム
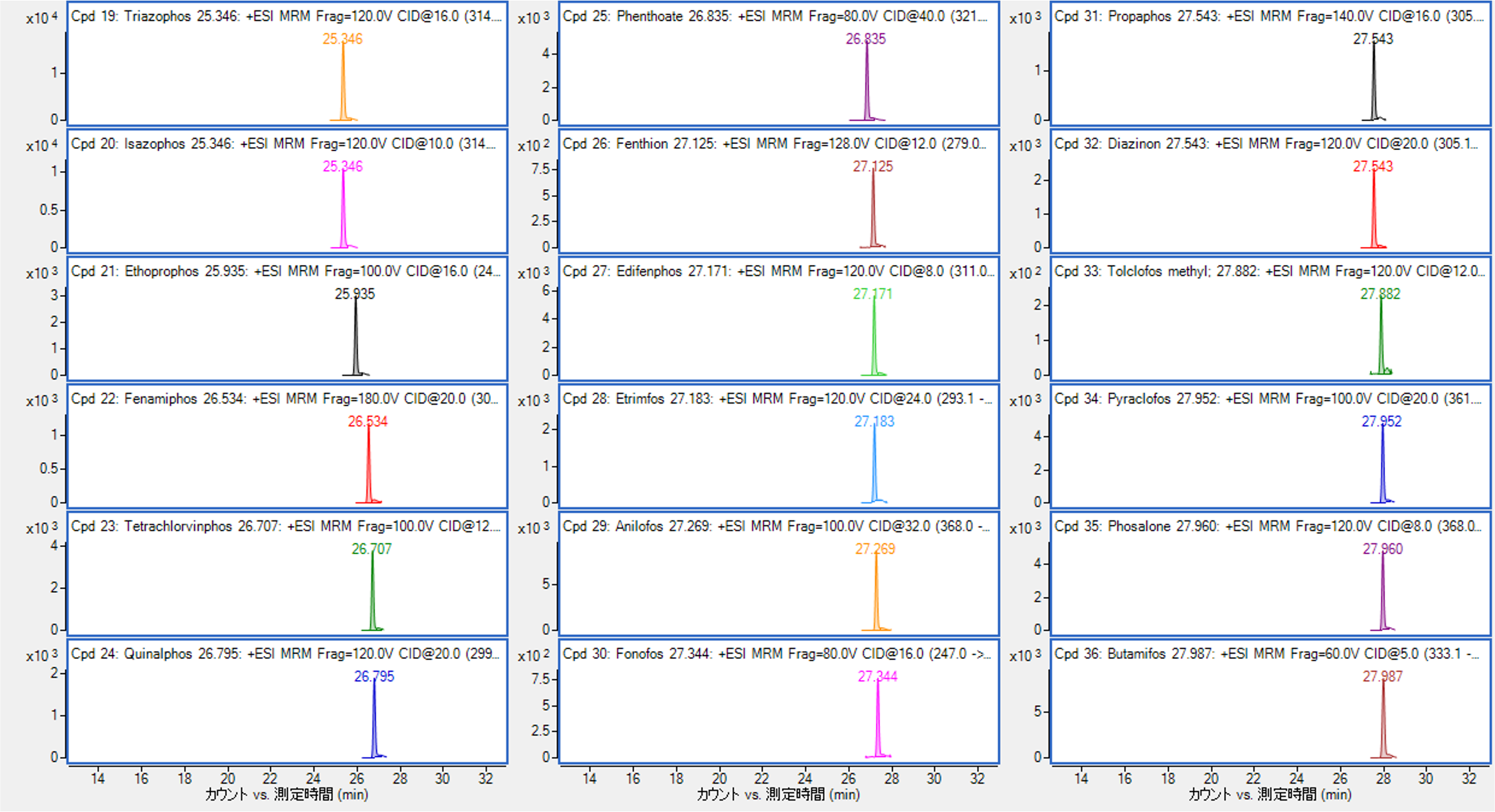
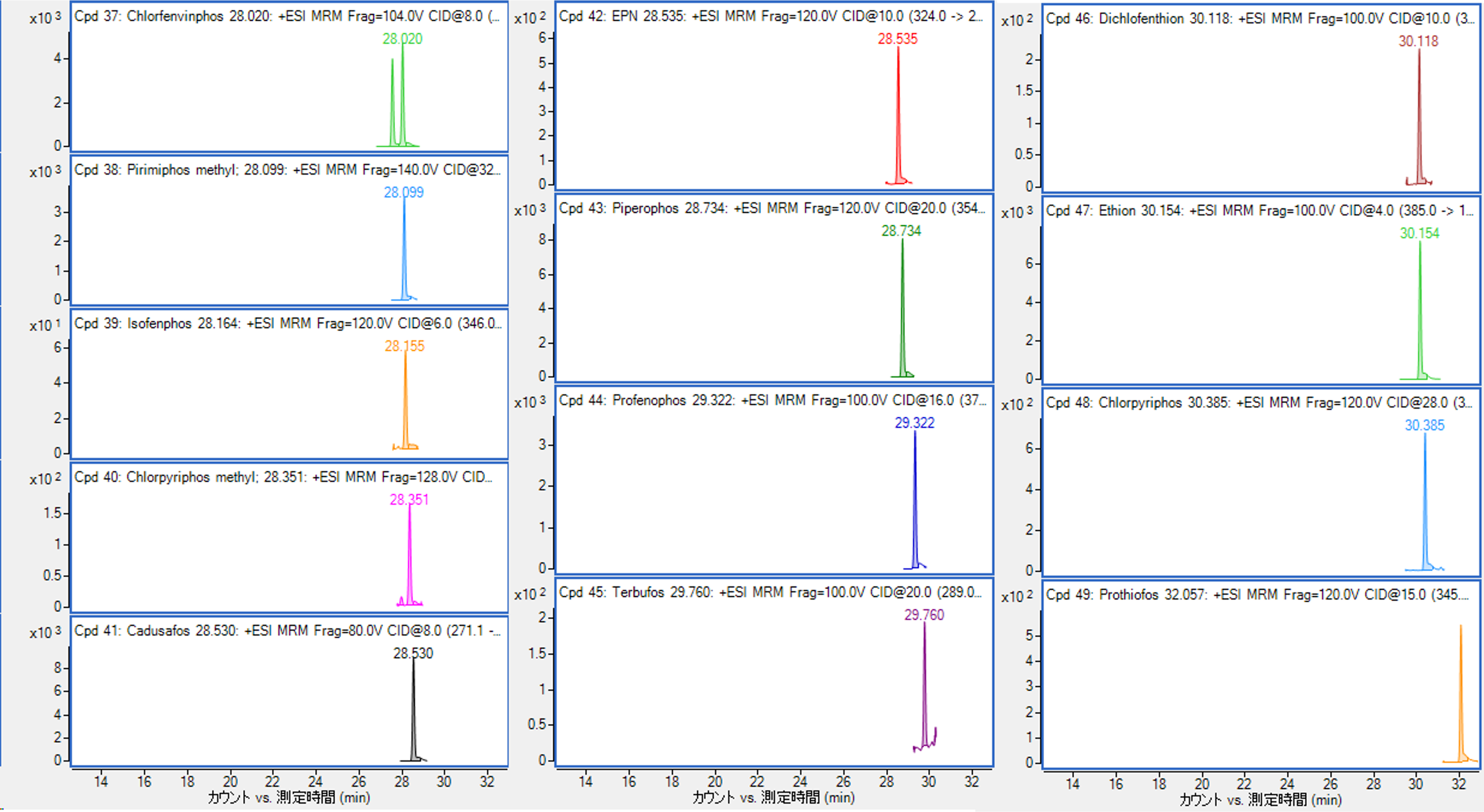 図1-2 GC/MS MixⅠ(1 ppb)のMRMクロマトグラム
図1-2 GC/MS MixⅠ(1 ppb)のMRMクロマトグラム
PL2005農薬GC/MS MixⅡ
表7に判定結果、図2に1 ppbでのMRMクロマトグラムを示した。49農薬中41農薬の測定が可能であったが、シフルトリンは1ppbでS/N<10であった(10 ppbで測定可能)。ベンフルラリン、ブロムプロピレート、ブロモホスメチル、ジメチピン、エンドスルファン、フェンクロルホス及びフサライドの測定が困難であった。
表7 GC/MS MixⅡの農薬及び判定結果
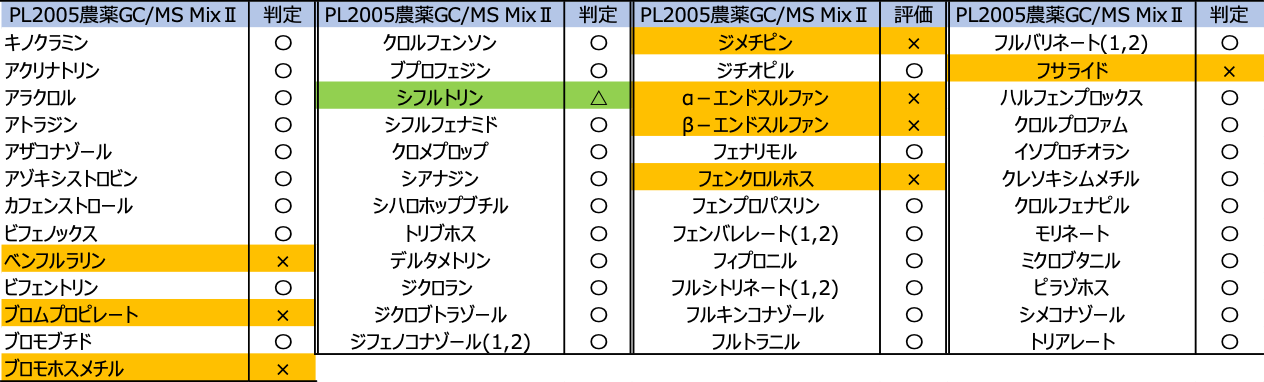

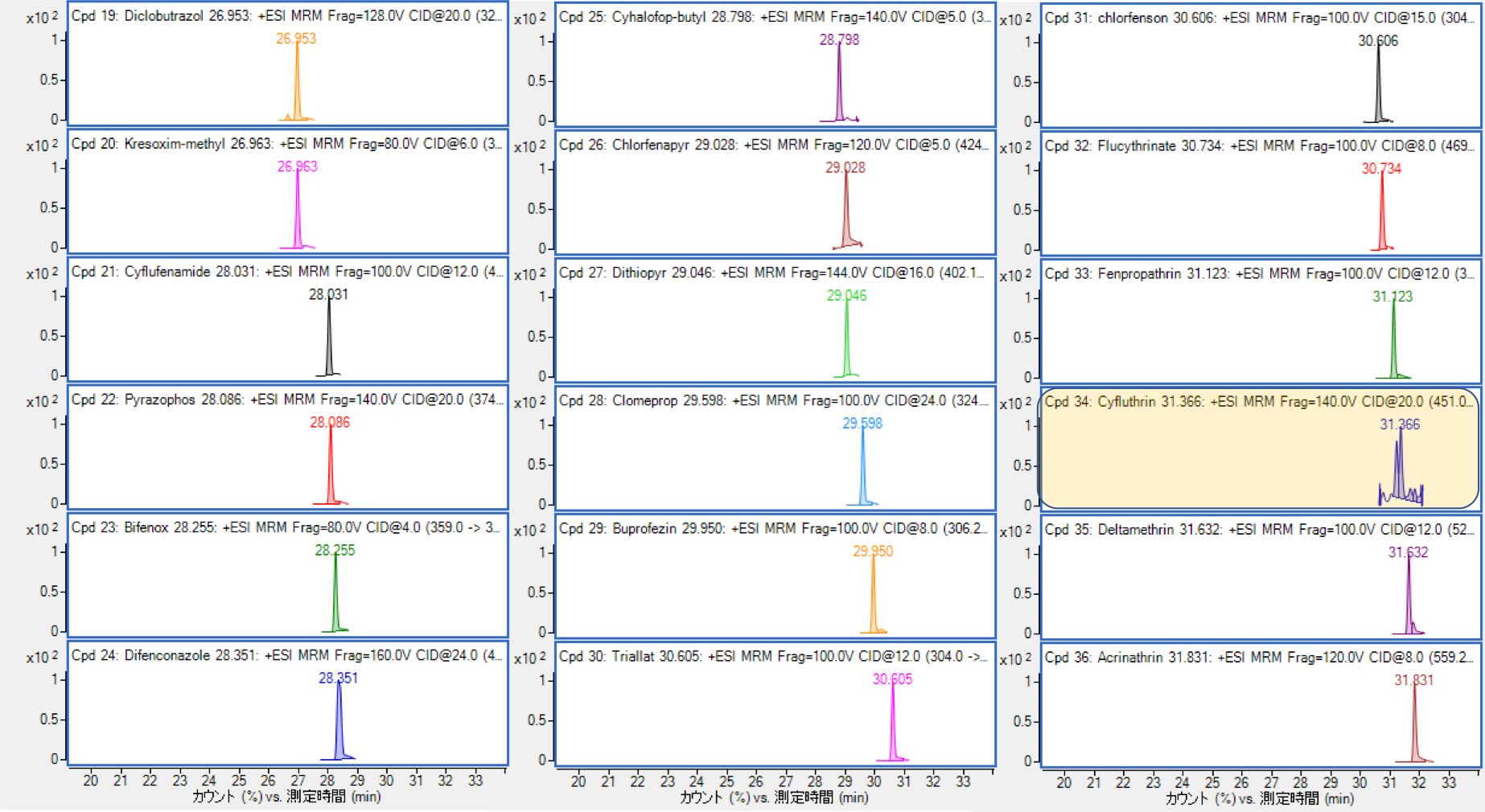
図2-1 GC/MS MixⅡ(1 ppb)のMRMクロマトグラム
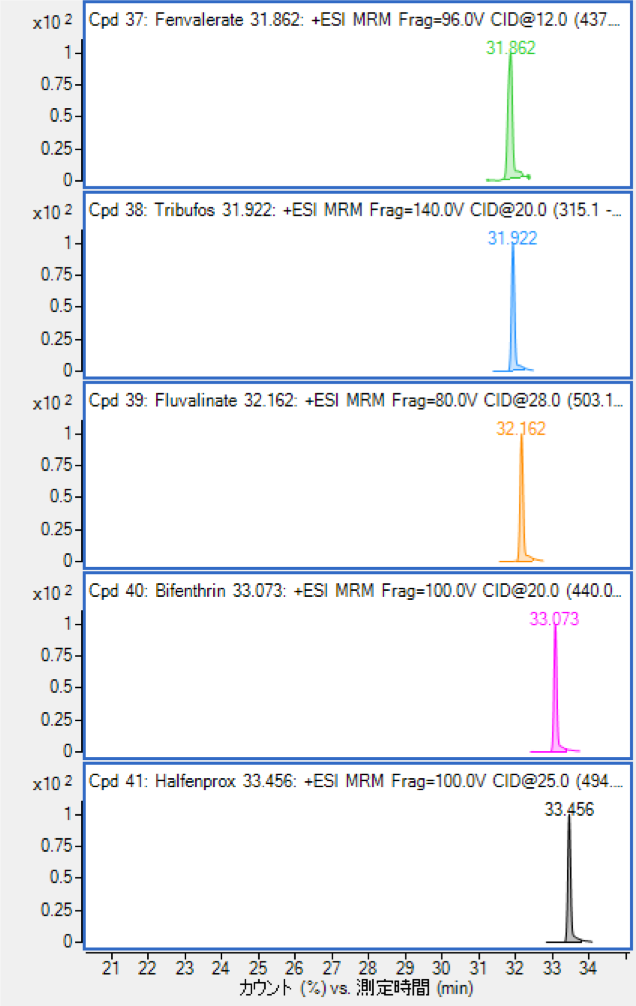
図2-2 GC/MS MixⅡ(1 ppb)のMRMクロマトグラム
PL2005農薬GC/MS Mix Ⅲ
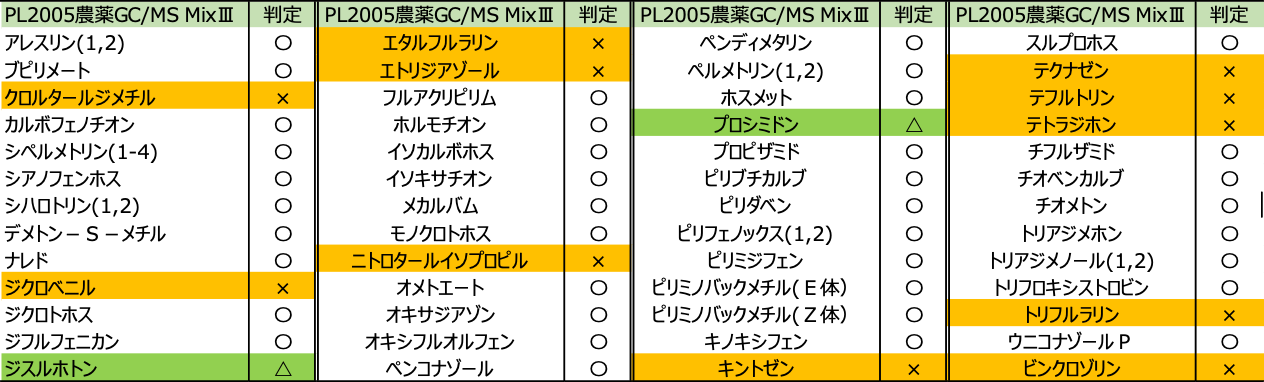
表8に判定結果、図3に1 ppbでのMRMクロマトグラムを示した。52農薬中41農薬の測定が可能であったが、ジスルホトン及びプロシミドンは1 ppbでS/N<10であった(両農薬共に10 ppbで測定可能)。クロルタールジメチル、ジクロベニル、エタフルラリン、エトリジアゾール、ニトロタールイソプロピル、キントゼン、テクナゼン、テフルトリン、テトラジホン、トリフルラリン及びピンクロゾリンの測定が困難であった。
表8 GC/MS Mix Ⅲの農薬及び判定結果
今回の測定の際に全ての混合標準液はメタノールで希釈したが、GC/MS Mix Ⅲ中のホルモチオンはScanモードでは十分な強度で検出されたが、MRMモードでは極端に強度が低かった。そこで2 ppm農薬混合標準液を10時間の間隔で2回測定を行った。
その結果、図4に示した通りメタノール溶液ではホルモチオンの強度が10時間後には大きく低下していた。ホルモチオンはGCの注入口で熱分解し、ジメトエートに変換されるとの報告がある事から1)、メタノールとアセトニトリルで希釈した0.2ppm農薬混合標準液を6時間後、ジメトエートのdMRM条件を追加したdMRM法で測定を行った。
結果は図5に示したが、メタノール溶液ではホルモチオンは検出されず、ジメトエートが検出された。一方、アセトニトリル溶液では、ジメトエートは検出されず、ホルモチオンが検出された事から、メタノール中でホルモチオンはジメトエートに分解し、アセトニトリル中では安定であると考えられる。従って、GC/MS Mix Ⅲはアセトニトリルで希釈して測定を行った。
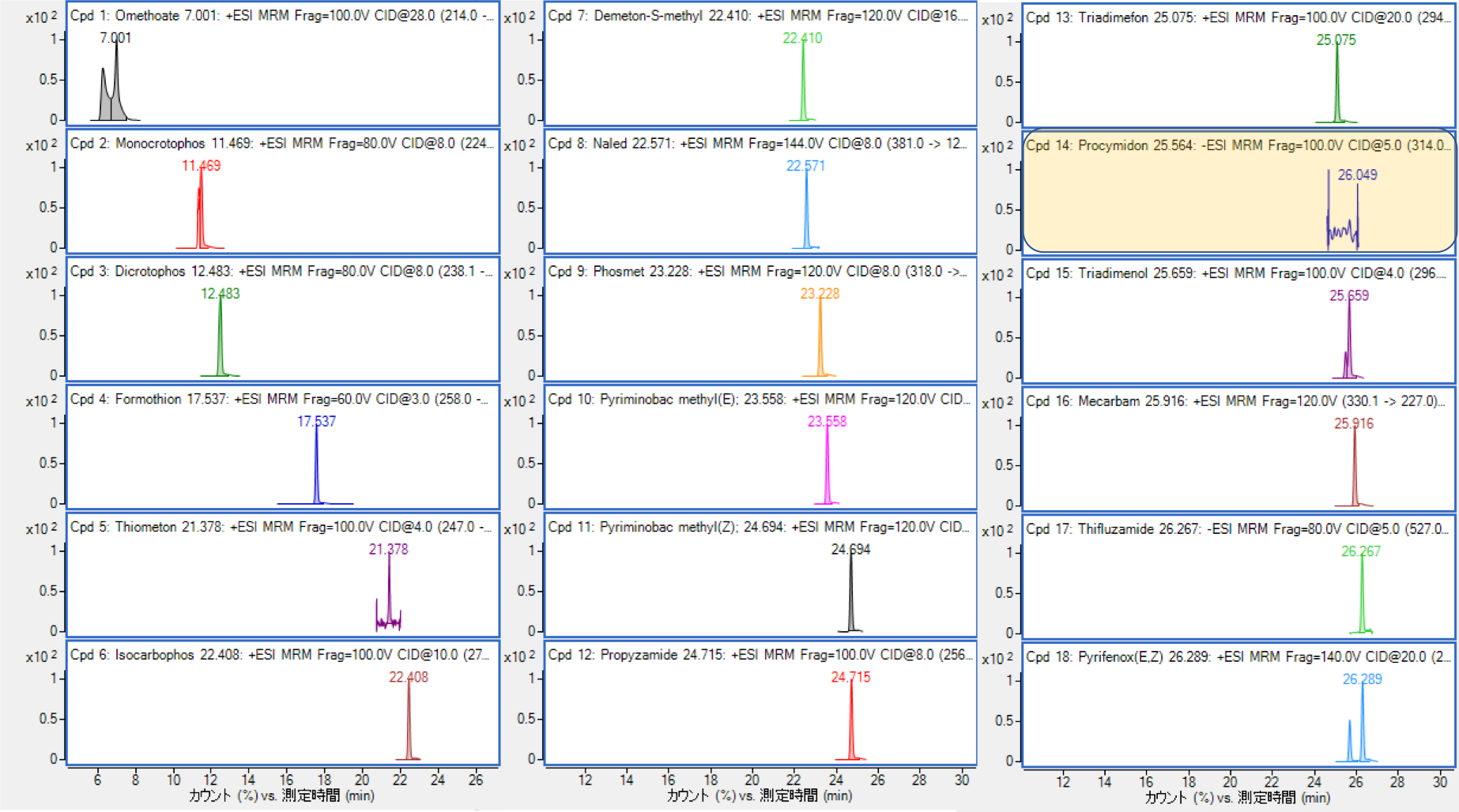
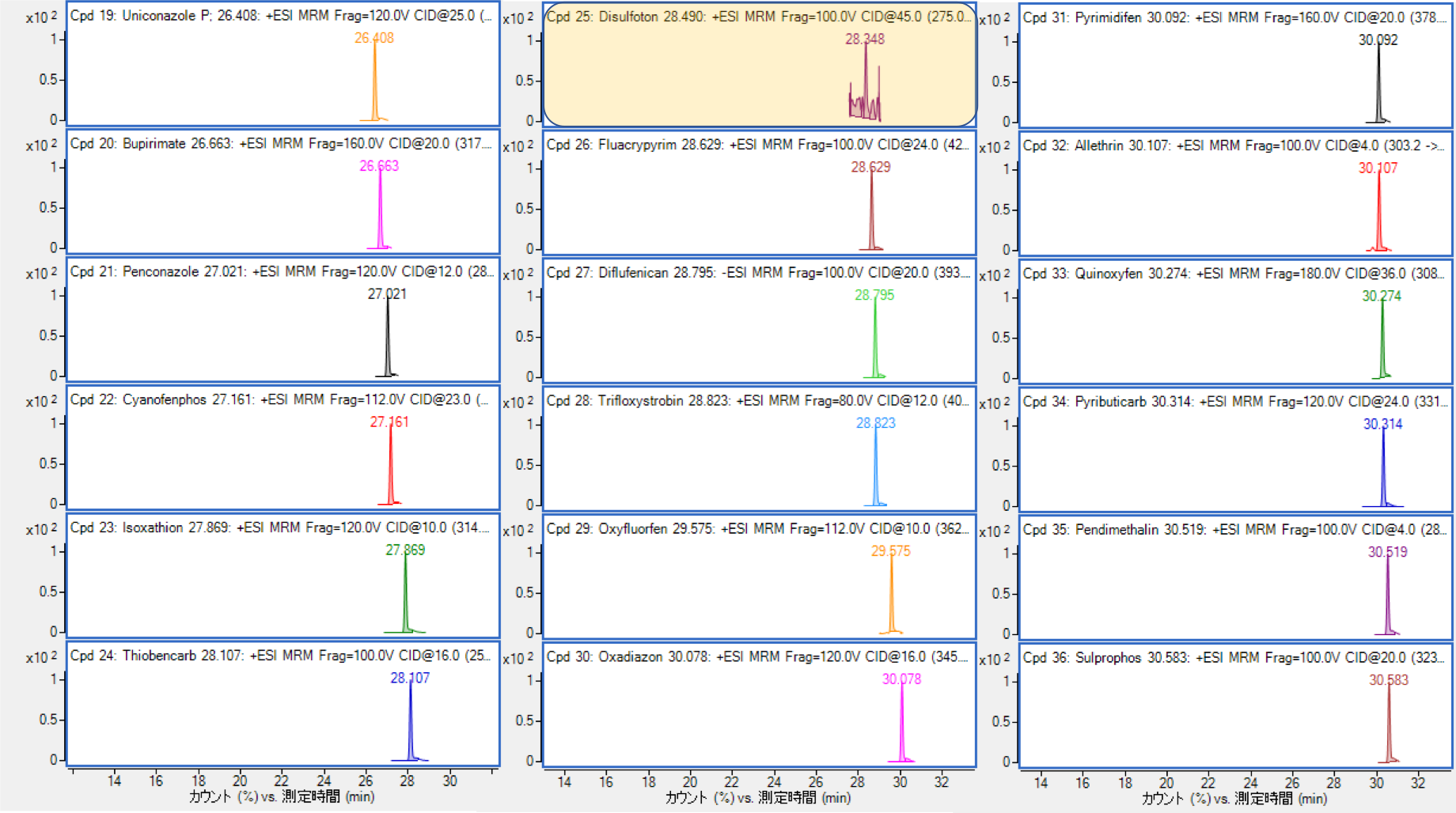
図3-1 GC/MS Mix Ⅲ(1 ppb)のMRMクロマトグラム
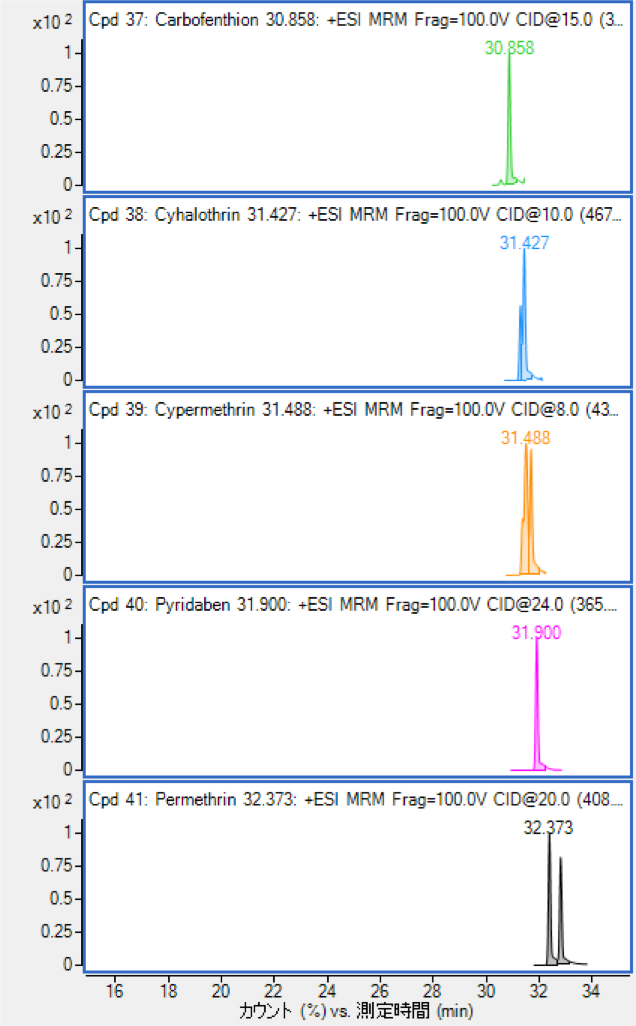
図3-2 GC/MS Mix Ⅲ(1 ppb)のMRMクロマトグラム
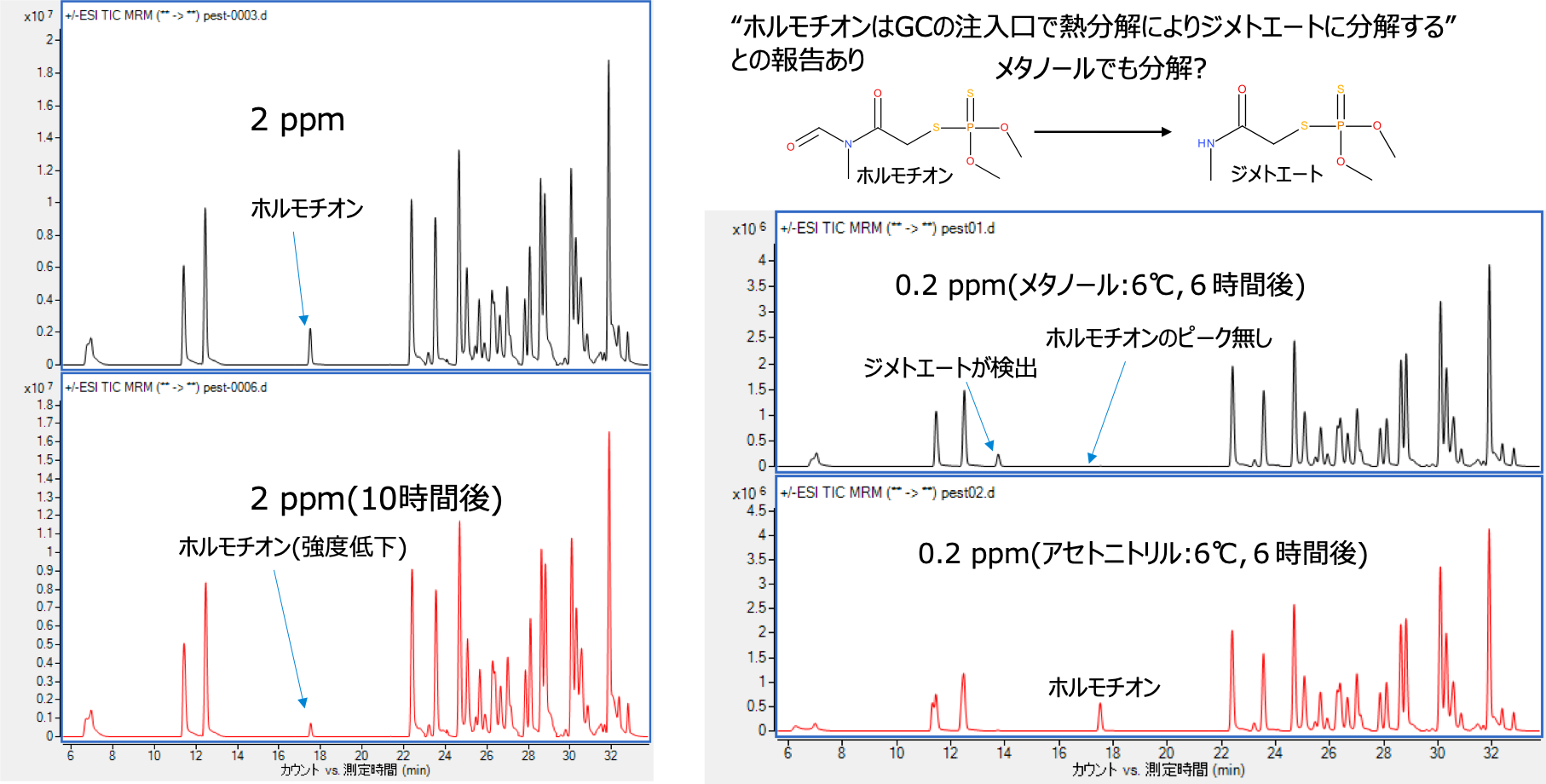 図4 メタノール溶液でのGC/MS Mix ⅢのTIC(2 ppm)
図5 メタノール及びアセトニトリル溶液でのGC/MS Mix Ⅲ(0.2 ppm)のMRMクロマトグラム
図4 メタノール溶液でのGC/MS Mix ⅢのTIC(2 ppm)
図5 メタノール及びアセトニトリル溶液でのGC/MS Mix Ⅲ(0.2 ppm)のMRMクロマトグラム
*本記事は2024年1月に執筆いただいた情報です。
Profile
滝埜 昌彦氏
アジレント・テクノロジー株式会社(https://www.chem-agilent.com/)
クロマトグラフィー・質量分析営業部門
(LC・LC/MSグループ)
シニアアプリケーションスペシャリスト
学歴
京都薬科大学 製薬化学科 卒業
大阪府立大学 大学院 工学研究科 博士後期課程 物質系専攻 応用化学分野 修了(博士(工学))
会員特典「GC/MS混合標準液の分析」PDFでダウンロード
今回、ご紹介したアジレント・テクノロジー株式会社 滝埜 昌彦氏 著「GC/MS混合標準液の分析」をPDFにてダウンロードいただけます。
※閲覧・ダウンロードには試薬ダイレクトの会員登録が必要です。

後編はこちら
 後編
後編
【会員特典付き】GC/MS混合標準液の分析 後編
GC-MS用農薬混合標準液(当社製品、PL2005農薬GC/MS Mix Ⅳ,Ⅴ,Ⅵ,7)を用いて、LC-MSで測定を行い測定に適しているかの評価を行っていただきました。